円板状エリテマトーデス(DLE)は、主に皮膚に症状が現れる自己免疫疾患の一種で、頭皮に発症すると瘢痕性の脱毛を引き起こすことがあります。
 Dr.小林智子
Dr.小林智子この記事では、DLE性脱毛症の詳しい原因と、皮膚科で行われる専門的な検査方法について解説します。
免疫異常が導く自己炎症 DLE性脱毛症の根本原因
DLE性脱毛症は、免疫システムが自身の体の組織、特に毛包を誤って攻撃することで引き起こされると考えられています。この自己免疫反応が慢性的な炎症を誘発し、毛包の破壊と瘢痕化を招き、結果として永久的な脱毛に至ります。
根本的な原因の理解は、より良い対処法を見つける第一歩です。
自己免疫応答の異常
健康な状態では、免疫システムは細菌やウイルスなどの外敵から体を守る役割を担います。しかし、DLEのような自己免疫疾患では、このシステムに異常が生じ、自身の細胞や組織を「異物」と認識して攻撃を始めてしまいます。
DLE性脱毛症の場合、毛包がその標的となります。
Tリンパ球の役割
免疫細胞の一種であるTリンパ球は、細胞性免疫において中心的な役割を果たします。DLEの病変部では、これらのTリンパ球が異常に活性化し、毛包周囲に集まっていることが確認されています。
これらの細胞が放出する炎症性サイトカイン(細胞間の情報伝達物質)が、毛包へのダメージを増幅させると考えられています。
Bリンパ球と自己抗体
Bリンパ球は抗体を産生する免疫細胞です。DLE患者さんの中には、自己の細胞成分に対する抗体(自己抗体)が検出されることがあります。
これらの自己抗体が直接的に毛包を攻撃するのか、あるいは炎症プロセスを間接的に悪化させるのかについては、まだ研究が進められています。
全身性エリテマトーデス(SLE)への移行リスクも考慮し、これらのマーカーを注視することが大切です。
炎症性サイトカインの影響
炎症性サイトカインは、免疫細胞から放出されるタンパク質で、炎症反応の調節に深く関わっています。DLEの病態においては、これらのサイトカインのバランスが崩れ、過剰な炎症が持続する原因となります。
インターフェロンの関与
特にDLEでは、インターフェロンと呼ばれるサイトカイン群が重要な役割を果たすと考えられています。
紫外線暴露などがきっかけとなり、皮膚細胞からインターフェロンが過剰に産生されると、免疫細胞が活性化されやすくなり、自己免疫反応が惹起される可能性があります。このため、紫外線対策はDLEの管理において非常に重要です。
炎症による毛包破壊
持続的な炎症は、毛包の正常な構造と機能を徐々に破壊していきます。初期には可逆的な変化であっても、炎症が長期化すると毛包は線維組織に置き換わり(瘢痕化)、毛髪を再生する能力を永久に失ってしまいます。
このため、早期に炎症を抑える治療が求められます。ステロイド外用薬や、場合によっては免疫抑制剤の内服が検討されます。
紫外線・ホルモン・遺伝要因 発症を後押しする三大トリガー
DLE性脱毛症の発症には、個人の免疫システムの特性に加え、いくつかの環境因子や内的因子が関与していると考えられています。これらを理解することは、発症予防や症状悪化の防止につながります。
紫外線暴露と皮膚への影響
紫外線はDLEの最もよく知られた増悪因子の一つです。紫外線は皮膚細胞にダメージを与え、炎症反応を引き起こすだけでなく、免疫システムを刺激して自己免疫反応を誘発する可能性があります。
紫外線A波・B波の作用
紫外線にはA波(UVA)とB波(UVB)があり、どちらも皮膚に影響を与えます。UVBは表皮に強く作用し、DNA損傷や炎症を引き起こしやすいとされます。UVAは皮膚のより深い層まで到達し、長期的な影響を及ぼす可能性があります。
DLE患者さんは、季節を問わず徹底した紫外線対策が必要です。
光線過敏症のメカニズム
DLE患者さんの一部には、光線過敏症が見られます。これは、紫外線に暴露された皮膚細胞がアポトーシス(プログラムされた細胞死)を起こしやすくなり、その際に放出される自己抗原が免疫系を刺激するためと考えられています。
日焼け止めの使用、帽子や日傘の活用が推奨されます。
女性ホルモンの関与の可能性
DLEは男性よりも女性に多く見られる傾向があり、特に妊娠可能な年齢層での発症が多いことから、女性ホルモンが何らかの形で関与している可能性が指摘されています。
しかし、その詳細な関連性についてはまだ完全には解明されていません。
エストロゲンと免疫応答
エストロゲンは免疫系の調節に関与しており、特定の条件下では自己免疫反応を促進する方向に働く可能性が示唆されています。
妊娠や経口避妊薬の使用などが、一部の患者さんで症状に影響を与えることも報告されていますが、個人差が大きいです。
遺伝的素因と家族歴
DLEの発症には遺伝的な要素も関わっていると考えられています。
特定の遺伝子を持つ人がDLEを発症しやすい可能性が研究されていますが、単一の遺伝子で決まるわけではなく、複数の遺伝子と環境因子が複雑に絡み合って発症に至ると考えられています。
HLAタイプとの関連
ヒト白血球抗原(HLA)は、免疫システムが自己と非自己を認識するのに重要な役割を果たす分子です。特定のHLAタイプとDLEを含む自己免疫疾患との関連が指摘されており、遺伝的背景が発症リスクに影響する一因とされています。
ただし、関連するHLAタイプを持っていても必ず発症するわけではありません。
以下の表は、DLE性脱毛症の発症に関与する可能性のある要因をまとめたものです。
DLE発症に関わる可能性のある要因
| 要因カテゴリ | 具体的要因 | 影響の概要 |
|---|---|---|
| 環境因子 | 紫外線 | 皮膚細胞の損傷、免疫系の活性化 |
| 内的因子 | 女性ホルモン(可能性) | 免疫応答への影響(詳細は研究中) |
| 遺伝的素因 | 特定のHLAタイプなど | 自己免疫疾患への罹患しやすさ |
自己抗体と補体活性 血液マーカーが示す病態指標
DLE性脱毛症の診断や活動性の評価において、血液検査は重要な情報を提供します。特に、自己抗体の存在や補体系の活性化は、免疫系の異常を示す指標となります。
抗核抗体(ANA)の意義

抗核抗体(ANA)は、自己の細胞核の成分に対する抗体の総称です。DLE患者さんの約30-50%で陽性となると報告されていますが、ANA陽性が必ずしもDLEを意味するわけではなく、他の膠原病や健常者でも陽性になることがあります。
しかし、高い力価で陽性の場合や、特徴的な蛍光パターンを示す場合は、診断の一助となります。
ANAの検査法と解釈
ANAは通常、間接蛍光抗体法という方法で検査されます。
細胞をスライドグラスに固定し、患者さんの血液(血清)と反応させ、さらに蛍光標識された二次抗体を反応させることで、細胞核に対する抗体の有無と、その分布パターン(蛍光型)を観察します。
力価(希釈倍率)が高いほど、抗体の量が多いことを示唆します。
以下に代表的なANAの蛍光型と関連疾患を示します。
ANA蛍光型と主な関連疾患
| 蛍光型 | 主な関連疾患 | DLEでの陽性率 |
|---|---|---|
| Homogeneous (均質型) | SLE、薬剤誘発性ループス | 時に見られる |
| Speckled (斑紋型) | SLE、シェーグレン症候群、強皮症 | 時に見られる |
| Nucleolar (核小体型) | 強皮症、多発性筋炎/皮膚筋炎 | 稀 |
抗dsDNA抗体の特異性
抗二本鎖DNA(dsDNA)抗体は、全身性エリテマトーデス(SLE)に比較的特異性の高い自己抗体です。DLE患者さんでは通常陰性か低力価陽性ですが、高力価で陽性の場合、SLEへの移行リスクを考慮する必要があります。
皮膚科専門医は、皮膚症状だけでなく、全身症状の有無にも注意を払います。
補体系の変動
補体は、免疫反応において重要な役割を果たす血清タンパク質群です。自己抗体が組織に結合すると、補体が活性化され、炎症反応を増強したり、細胞を破壊したりします。
DLEの活動期には、補体成分(特にC3、C4)が消費されて血清中の値が低下することがあります。
CH50、C3、C4の測定
CH50は補体系全体の活性を、C3およびC4は個々の補体成分の量を反映します。これらの値が低下している場合、免疫複合体の形成や補体の活性化が亢進している可能性を示唆し、疾患の活動性と関連することがあります。
ただし、これらのマーカーはDLEに特異的なものではなく、他の炎症性疾患や自己免疫疾患でも変動します。
毛包周囲の線維化と血管変化 組織学が語る脱毛進行路
DLE性脱毛症の確定診断や進行度評価には、頭皮の組織を採取して顕微鏡で観察する皮膚生検が非常に重要です。組織学的所見は、脱毛がどのように進行しているか、炎症の程度、瘢痕化の有無などを詳細に明らかにします。
リンパ球浸潤と毛包炎
DLEの初期病変では、毛包周囲、特に毛包漏斗部や峡部にリンパ球を中心とした炎症細胞の浸潤が見られます。この炎症は毛包の細胞を傷害し(液状変性)、毛包の正常な構造を破壊していきます。これが「毛包炎」と呼ばれる状態です。
炎症細胞の種類と分布
主にCD4陽性Tリンパ球が主体ですが、CD8陽性Tリンパ球やBリンパ球、形質細胞なども見られることがあります。これらの細胞が毛包上皮やその周囲に密に集まっている像は、DLEに特徴的な所見の一つです。
基底膜の肥厚とムチン沈着
DLEの病変部では、表皮と真皮の境界にある基底膜が肥厚していることがよく観察されます。また、真皮内にムチンという酸性ムコ多糖類が沈着することも特徴的です。
これらの所見は、慢性的な炎症と組織修復反応の結果と考えられます。
毛包の破壊と瘢痕化
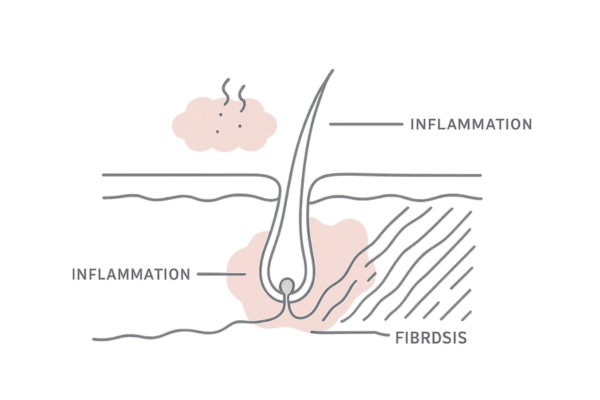
炎症が長期にわたると、毛包は徐々に破壊され、最終的には線維組織に置き換わります。これを瘢痕化と呼び、一度瘢痕化が完成すると、その部分から毛髪が再生することは困難になります。
これがDLE性脱毛症が瘢痕性脱毛症に分類される理由です。
線維化の程度と脱毛の不可逆性
皮膚生検では、線維化の範囲や程度を評価できます。早期に適切な治療(ステロイド外用や局所注射、免疫抑制剤など)を開始し、炎症をコントロールすることで、瘢痕化の進行を遅らせ、脱毛範囲の拡大を抑えることが期待できます。
しかし、進行した瘢痕に対しては、ウィッグの使用なども含めた整容的な改善策を検討することがあります。
以下は、DLEの組織学的所見の進行度を示したものです。
DLEの組織学的進行度
| 進行度 | 主な組織所見 | 毛髪再生の可能性 |
|---|---|---|
| 初期 | 毛包周囲のリンパ球浸潤、液状変性 | 治療により改善の可能性あり |
| 中期 | 基底膜肥厚、真皮ムチン沈着、軽度の線維化 | 一部で再生困難 |
| 後期 | 著明な毛包破壊、広範な瘢痕化 | 再生は困難 |
血管の変化
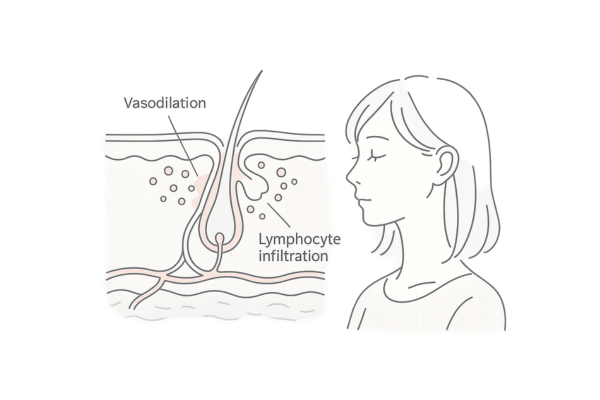
DLEの病変部では、毛細血管の拡張や血管壁の肥厚、血管周囲の炎症細胞浸潤なども見られることがあります。これらの血管変化も、炎症プロセスの維持や組織障害に関与していると考えられています。
まずは頭皮ダーモスコピー 在宅でも活かせる画像診断
ダーモスコピー(皮膚鏡検査)は、特殊な拡大鏡と光源を用いて皮膚の表面や浅い部分の構造を詳細に観察する非侵襲的な検査法です。DLE性脱毛症の初期診断や経過観察において、非常に有用な情報を提供します。
ダーモスコピー所見の特徴
DLE性脱毛症の頭皮では、ダーモスコピーで以下のような特徴的な所見が観察されることがあります。
- 角栓(毛孔一致性の黄色~白色の栓)
- 毛孔周囲の紅斑や色素沈着
- 樹枝状血管(不規則に拡張した血管)
- 白色瘢痕領域(瘢痕化した部分)
- 毛幹の太さの不同
これらの所見は、他の脱毛症との鑑別に役立ちます。特に角栓はDLEに比較的特徴的な所見とされています。
非侵襲的検査の利点
ダーモスコピーは痛みを伴わず、短時間で行えるため、患者さんの負担が少ない検査です。また、病変部を経時的に観察することで、治療効果の判定や再燃の早期発見にも役立ちます。
最近では、スマートフォンに取り付けて使用できる簡易的なダーモスコープもあり、専門医の指導のもとであれば、患者さん自身が自宅で頭皮の状態をチェックする際にも活用できる可能性があります。
ダーモスコピー所見の記録と共有
皮膚科では、ダーモスコピー画像を撮影して記録し、治療前後の変化を比較します。これにより、治療法の選択や調整がより客観的に行えます。
患者さん自身も画像を見ることで、自身の状態を理解しやすくなり、治療へのモチベーション向上にもつながります。
他の脱毛症との鑑別点
円形脱毛症や脂漏性皮膚炎に伴う脱毛など、他の脱毛症でもダーモスコピー所見に特徴が見られます。例えば、円形脱毛症では感嘆符毛(!)や黒点、黄色点などが特徴的です。皮膚科専門医はこれらの所見を総合的に判断し、診断を進めます。
以下の表は、ダーモスコピーで観察される主な所見と、それが示唆する状態をまとめたものです。
ダーモスコピー所見と示唆される状態
| ダーモスコピー所見 | 示唆される状態・疾患 | DLEでの特徴 |
|---|---|---|
| 角栓 | 毛孔の角化異常 | DLEで比較的よく見られる |
| 樹枝状血管 | 真皮の血管拡張 | DLE、基底細胞癌など |
| 白色瘢痕領域 | 瘢痕化 | 進行したDLE、他の瘢痕性脱毛症 |
採血でわかる活動性 ANA・dsDNA・補体価の読み解き方
DLE性脱毛症の診断補助や活動性の評価、全身性エリテマトーデス(SLE)への移行リスクの判断には、血液検査が重要な役割を果たします。特に自己抗体や補体価の測定は、免疫系の状態を把握する上で参考になります。
抗核抗体(ANA)のスクリーニング
前述の通り、ANAは自己免疫疾患のスクリーニングとして広く用いられます。DLE患者さんでは陽性率がそれほど高くないものの、高力価陽性や特定の蛍光型は診断の手がかりとなります。
特に、皮膚症状のみで他の全身症状がない場合でも、ANAが陽性であれば、潜在的な自己免疫素因を考慮します。
ANA力価と臨床症状の関連
ANAの力価(例:40倍、80倍、160倍など)が高いほど、自己免疫疾患の存在が強く疑われます。しかし、力価の高さと症状の重症度が必ずしも比例するわけではありません。
また、健常者でも低い力価(例:40倍、時に80倍)で陽性となることがあります。皮膚科専門医は、他の検査結果や臨床症状と合わせて総合的に判断します。
抗dsDNA抗体とSLEへの警戒
抗dsDNA抗体は、SLEに比較的特異性が高い自己抗体です。DLE患者さんでこの抗体が高力価陽性である場合、SLEを発症しているか、将来的に発症するリスクが高いと考えられます。
そのため、定期的な経過観察と、腎臓や関節など全身の症状についての問診が重要になります。
DLEからSLEへの移行
DLE患者さんの約5-10%がSLEに移行すると言われています。抗dsDNA抗体陽性、ANA高値、補体低値などは、そのリスク因子と考えられています。
早期にSLEの兆候を発見し、適切な治療(例えば、免疫抑制剤の強化など)を開始することで、重篤な臓器障害を防ぐことが期待できます。
補体価(C3、C4、CH50)の評価
補体は免疫反応で消費されるため、活動性の高い自己免疫疾患では血清中の補体価が低下することがあります。DLE単独では著明な補体低下は稀ですが、SLEを合併している場合や、疾患活動性が高い場合には低下が見られることがあります。
以下の表は、DLE性脱毛症に関連する主な血液検査項目とその意義をまとめたものです。
DLE関連の主要血液検査項目
| 検査項目 | 基準値の目安 | DLEにおける意義 |
|---|---|---|
| 抗核抗体(ANA) | 40倍未満 | 陽性の場合、自己免疫素因を示唆 |
| 抗dsDNA抗体 | 施設により異なる(例:7 IU/mL未満) | 高値の場合、SLE合併・移行を疑う |
| 補体価(C3, C4) | C3: 80-160 mg/dL, C4: 15-45 mg/dL (目安) | 活動期やSLE合併で低下の可能性 |
これらの血液検査の結果は、単独で診断を確定するものではなく、臨床症状、ダーモスコピー所見、皮膚生検の結果などと合わせて総合的に評価されます。
定期的な検査により、病状の変化や治療効果を把握し、治療方針の調整に役立てます。
確定診断には頭皮生検 病態を可視化する顕微鏡所見
DLE性脱毛症の診断を確定し、他の脱毛症と鑑別するためには、頭皮の一部を採取して顕微鏡で詳細に調べる皮膚生検が最も確実な方法です。これにより、病変の深さ、炎症の性質、瘢痕化の程度などを直接評価できます。
生検の手技と目的
頭皮生検は、局所麻酔下で通常直径2mmから4mm程度の小さな皮膚組織を採取する手技です。採取部位は、活動性の病変縁(赤みや鱗屑がある部分)や、脱毛が進行していると思われる領域から選択します。
目的は、DLEに特徴的な組織学的所見を確認し、他の瘢痕性脱毛症や非瘢痕性脱毛症との鑑別を行うことです。
生検部位の選定
最も診断的価値の高い情報が得られるよう、皮膚科専門医はダーモスコピー所見なども参考にしながら、慎重に生検部位を選びます。活動初期の病変と、進行した瘢痕化した病変では所見が異なるため、複数の部位から採取することもあります。
DLEに特徴的な組織学的所見
顕微鏡下で観察されるDLEの代表的な所見には、以下のようなものがあります。
- 表皮の萎縮と過角化、毛孔角栓
- 基底細胞層の液状変性
- 真皮乳頭層の浮腫
- 毛包周囲および血管周囲へのリンパ球主体の密な炎症細胞浸潤
- 基底膜の肥厚(PAS染色で明瞭化)
- 真皮のムチン沈着(アルシアンブルー染色で陽性)
- 進行例では毛包の破壊と線維化(瘢痕形成)
これらの所見が揃うことで、DLEの診断はより確実なものとなります。
直接免疫蛍光法(DIF)
皮膚生検の検体を用いて、直接免疫蛍光法(DIF)という特殊な検査を行うこともあります。これは、組織内に沈着している免疫グロブリン(IgG, IgM, IgAなど)や補体成分(C3など)を蛍光顕微鏡で検出する方法です。
DLEの病変部では、表皮と真皮の境界部(基底膜部)にこれらの免疫複合体が帯状に沈着している像(ループスバンドテスト陽性)が見られることがあり、診断の補助となります。
以下の表は、DLEの皮膚生検における主な組織学的所見とDIF所見をまとめたものです。
DLEの皮膚生検所見まとめ
| 検査方法 | 主な所見 | 診断への寄与 |
|---|---|---|
| 通常染色 (H&E) | 毛包周囲リンパ球浸潤、基底層液状変性、毛孔角栓、線維化 | 炎症のパターンと瘢痕化の評価 |
| 特殊染色 (PAS, アルシアンブルー) | 基底膜肥厚、ムチン沈着 | DLEに特徴的な変化の確認 |
| 直接免疫蛍光法 (DIF) | 表皮真皮境界部への免疫グロブリン・補体沈着 | 免疫学的機序の確認、SLEとの関連評価 |
皮膚生検は侵襲的な検査ですが、得られる情報は非常に多く、治療方針の決定にも大きく影響します。担当の皮膚科医とよく相談し、検査の必要性や手技について理解を深めることが大切です。
他の瘢痕性脱毛症との鑑別 見落としを防ぐチェックポイント
DLE性脱毛症は瘢痕性脱毛症の一つですが、他にも毛包を破壊し永久的な脱毛を引き起こす疾患がいくつか存在します。正確な診断のためには、これらの疾患との鑑別が重要です。
毛孔性扁平苔癬(LPP)
毛孔性扁平苔癬は、頭皮に好発する瘢痕性脱毛症で、DLEとしばしば鑑別が必要になります。毛孔周囲の紅斑や軽度の鱗屑、毛孔の消失を特徴とし、組織学的には毛包漏斗部から峡部にかけてリンパ球浸潤が見られます。
DLEとの違いは、DIFで免疫グロブリンの沈着パターンが異なることや、ムチン沈着が通常見られない点などです。
LPPのダーモスコピー所見
LPPでは、毛孔周囲の白色の鱗屑(perifollicular scaling)や、青灰色の色素沈着(blue-gray dots)が特徴的なダーモスコピー所見とされます。これらの所見はDLEとの鑑別に役立ちます。
偽瘢痕性脱毛症(Brocq)
かつて独立した疾患と考えられていましたが、現在ではLPPやDLEなどの最終的な瘢痕状態を指すことが多いとされています。特徴的な臨床像や組織像に乏しく、診断は除外診断的に行われることがあります。
禿髪性毛包炎(Folliculitis Decalvans)
主に頭頂部に生じる慢性的な化膿性の毛包炎で、多発する膿疱、びらん、痂皮形成を伴い、最終的に瘢痕性脱毛に至ります。
細菌感染(特に黄色ブドウ球菌)が関与していると考えられており、DLEとは炎症の主体(好中球が目立つ)や臨床像が異なります。
以下の表は、主な瘢痕性脱毛症の鑑別点を示したものです。
主な瘢痕性脱毛症の鑑別ポイント
| 疾患名 | 主な臨床的特徴 | 組織学的特徴(一部) |
|---|---|---|
| DLE性脱毛症 | 境界明瞭な紅斑、鱗屑、毛孔角栓、萎縮 | 液状変性、基底膜肥厚、ムチン沈着 |
| 毛孔性扁平苔癬 (LPP) | 毛孔周囲の紅斑・鱗屑、そう痒 | 毛包周囲の帯状リンパ球浸潤 |
| 禿髪性毛包炎 | 膿疱、痂皮、束毛 | 好中球主体の毛包炎、形質細胞浸潤 |
その他の鑑別疾患
中心性遠心性瘢痕性脱毛症(CCCA)は、主にアフリカ系女性の頭頂部に見られる瘢痕性脱毛症です。また、外傷や熱傷、放射線皮膚炎などによる二次的な瘢痕性脱毛も鑑別が必要です。
皮膚科専門医は、詳細な問診、視診、ダーモスコピー、そして必要に応じて皮膚生検を行い、これらの疾患を慎重に鑑別します。正確な診断が、適切な治療法選択と予後の改善につながります。
よくある質問
- DLE性脱毛症の原因はストレスですか
-
直接的な原因は自己免疫異常ですが、精神的・身体的ストレスは免疫系に影響を与え、症状を悪化させる可能性があります。ストレス管理も治療の一環として重要です。
- DLE性脱毛症は遺伝しますか
-
DLEそのものが直接遺伝するわけではありませんが、発症しやすい体質(遺伝的素因)は受け継がれる可能性があります。
血縁者に自己免疫疾患の方がいる場合は、発症リスクが一般より高いと考えられますが、必ず発症するわけではありません。
- 紫外線対策は夏だけで良いですか
-
いいえ、紫外線は一年中降り注いでいます。DLEの患者さんは、季節や天候に関わらず、日常的に紫外線対策(日焼け止め、帽子、日傘など)を行うことが推奨されます。特に頭皮は日光が当たりやすいため、注意が必要です。
- DLE性脱毛症と診断されたら、全身性エリテマトーデス(SLE)にもなりますか
-
DLE患者さんの全てがSLEに移行するわけではありません。約5-10%程度がSLEに移行すると言われています。皮膚科専門医による定期的な診察と検査(血液検査など)を受け、全身症状の有無を確認していくことが大切です。
- 頭皮生検は痛いですか。傷跡は残りますか
-
頭皮生検は局所麻酔をしてから行うため、検査中の痛みはほとんどありません。麻酔の注射の際にチクッとした痛みを感じる程度です。
採取する皮膚は通常2~4mm程度と小さいため、傷跡はほとんど目立たなくなりますが、体質によっては小さな瘢痕として残ることもあります。詳しくは担当医にご相談ください。
この記事ではDLE性脱毛症の原因と検査方法について解説しました。具体的な治療法や予防策については、以下の記事で詳しくご紹介しています。合わせてお読みいただき、より深い理解にお役立てください。
参考文献
ŻYCHOWSKA, Magdalena; ŻYCHOWSKA, Małgorzata. Dermoscopy of discoid lupus erythematosus–a systematic review of the literature. International Journal of Dermatology, 2021, 60.7: 818-828.
GOWDA, Shreya K., et al. Trichoscopic Features of Scalp Discoid Lupus Erythematosus versus Lichen Planopilaris: A Systematic Review. Clinical, Cosmetic and Investigational Dermatology, 2024, 805-827.
MILAN, Elisa; VEZZONI, Roberta; STARACE, Michela VR. Trichoscopy of Discoid Lupus Erythematosus in Caucasian Scalp: A Review. Skin Appendage Disorders, 2024, 10.5: 363-369.
UDOMPANICH, Siriorn; CHANPRAPAPH, Kumutnart; SUCHONWANIT, Poonkiat. Hair and scalp changes in cutaneous and systemic lupus erythematosus. American journal of clinical dermatology, 2018, 19: 679-694.
PATHAK, Jaya. The Role of Dermoscopy in the Diagnosis of Cicatricial and Non-Cicatricial Alopecias. 2014. PhD Thesis. Rajiv Gandhi University of Health Sciences (India).
UCHIYAMA, Masaki. Primary cicatricial alopecia: recent advances in evaluation and diagnosis based on trichoscopic and histopathological observation, including overlapping and specific features. The Journal of Dermatology, 2022, 49.1: 37-54.
KNIGHT, Lauren Kerry. Does alopecia have diagnostic weight in systemic lupus erythematosus?. 2022.
CONCHA, Josef Symon Salgado; WERTH, Victoria P. Alopecias in lupus erythematosus. Lupus science & medicine, 2018, 5.1: e000291.
KINOSHITA-ISE, Misaki; FUKUYAMA, Masahiro; OHYAMA, Manabu. Recent advances in understanding of the etiopathogenesis, diagnosis, and management of hair loss diseases. Journal of Clinical Medicine, 2023, 12.9: 3259.
PINEDO-MORALEDA, Fernando; TRISTÁN-MARTÍN, Belén; DRADI, Giulia Greta. Alopecias: practical tips for the management of biopsies and main diagnostic clues for general pathologists and dermatopathologists. Journal of Clinical Medicine, 2023, 12.15: 5004.
円板状エリテマトーデス(DLE)性脱毛症の関連記事





