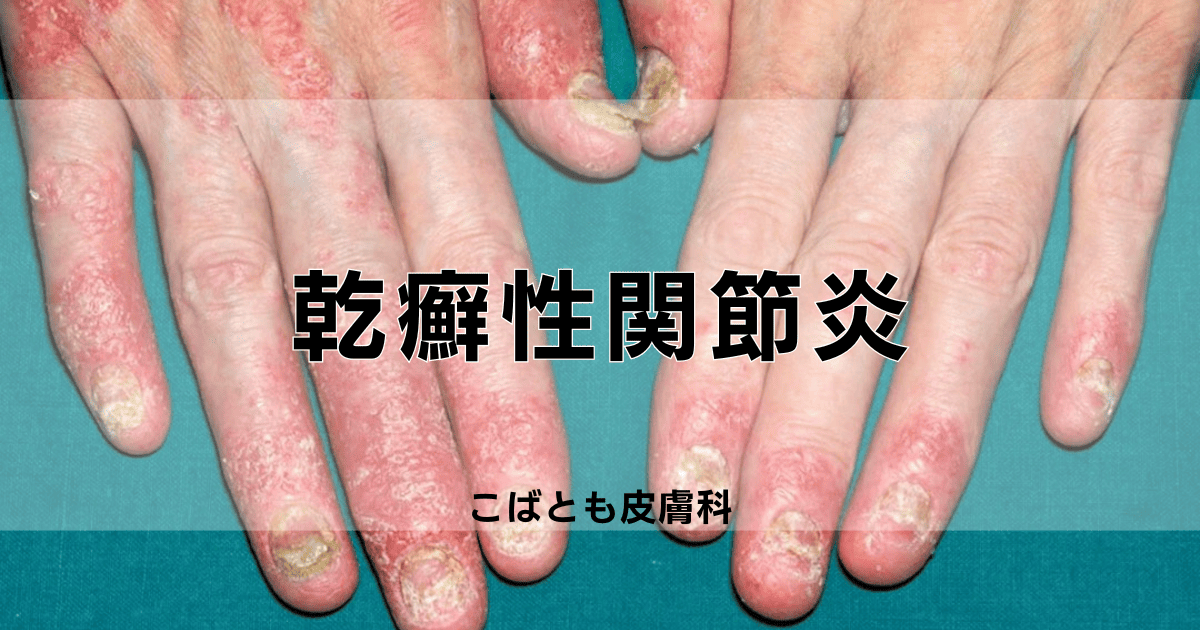
乾癬性関節炎(psoriatic arthritis)とは、乾癬患者さんの一部に見られる慢性的な炎症性関節疾患です。
この疾患は、皮膚の乾癬症状に加えて、関節の痛みや腫れを引き起こします。
乾癬性関節炎は、単なる皮膚の問題ではなく、全身に影響を及ぼす自己免疫疾患であり、早期発見と対応が重要です。
この記事の執筆者

小林 智子(こばやし ともこ)
日本皮膚科学会認定皮膚科専門医・医学博士
こばとも皮膚科院長
2010年に日本医科大学卒業後、名古屋大学医学部皮膚科入局。同大学大学院博士課程修了後、アメリカノースウェスタン大学にて、ポストマスターフェローとして臨床研究に従事。帰国後、同志社大学生命医科学部アンチエイジングリサーチセンターにて、糖化と肌について研究を行う。専門は一般皮膚科、アレルギー、抗加齢、美容皮膚科。雑誌を中心にメディアにも多数出演。著書に『皮膚科医が実践している 極上肌のつくり方』(彩図社)など。
こばとも皮膚科関連医療機関
乾癬性関節炎の病型
乾癬性関節炎は、末梢関節炎型、末梢関節炎型、末梢関節炎型、遠位指節間関節炎型、関節炎性変形性関節症型、に分類されます。
末梢関節炎型
末梢関節炎型は乾癬性関節炎の中で最も一般的な病型です。
この型では、手指や足趾の関節に加え、手首、肘、膝、足首などの大きな関節も影響を受け、対称性または非対称性の関節炎が見られます。
| 特徴 | 詳細 |
| 好発部位 | 手指、足趾、手首、肘、膝、足首 |
| 対称性 | 対称性または非対称性 |
| 頻度 | 最も一般的 |
脊椎関節炎型
脊椎関節炎型は、主に脊椎や仙腸関節に影響を与える病型で、背中や首の痛み、硬直感が特徴的です。
脊椎の可動性が制限されることもあり、長期的には脊椎の変形につながる可能性があります。
遠位指節間関節炎型
遠位指節間関節炎型は、指や足の爪に最も近い関節(遠位指節間関節)に炎症が生じる病型で、乾癬性関節炎に特徴的な爪の変化を伴うことが多いです。
遠位指節間関節の腫れや変形が見られ、日常生活での細かい動作に支障をきたすことがあります。
関節炎性変形性関節症型
関節炎性変形性関節症型は、主に大きな関節に影響を与える病型です。
この型では、関節の炎症に加えて、変形性関節症に似た変化が見られます。
| 病型 | 主な影響部位 |
| 末梢関節炎型 | 手指、足趾、大関節 |
| 脊椎関節炎型 | 脊椎、仙腸関節 |
| 遠位指節間関節炎型 | 指・足の爪に最も近い関節 |
| 関節炎性変形性関節症型 | 大関節 |
| 関節切断型 | 指・足趾の末端 |
関節切断型
関節切断型は、乾癬性関節炎の中でも最も重度な病型の一つで、指や足趾の末端部分が徐々に短くなっていく特徴があります。
関節切断型の主な特徴
- 指や足趾の末端部分が徐々に短縮
- 骨の吸収や軟部組織の萎縮が進行
- 爪の変形や脱落を伴うことが多い
- 機能障害や外観の変化が顕著
乾癬性関節炎の症状
乾癬性関節炎は、病型ごとに症状の現れ方や程度が大幅に異なります。
末梢関節炎型
この型は手足の小さな関節に影響を及ぼします。
主な症状
- 関節の痛みと腫れ
- 朝のこわばり
- 関節の動きにくさ
- 疲労感
手指や足趾の関節が左右非対称に腫れることが多く、乾癬性関節炎の特徴的な症状の一つです。
脊椎関節炎型
脊椎関節炎型は、背骨や仙腸関節に炎症を引き起こします。
主な症状
| 症状 | 特徴 |
| 背中の痛み | 慢性的で、特に朝に悪化 |
| 脊柱の硬直 | 徐々に進行する可能性あり |
| 頚部の痛み | 首の動きが制限される場合も |
| 仙腸関節の痛み | 臀部や腰の痛みとして現れる |
この型では、炎症が脊椎の靭帯や腱の付着部にも及ぶことがあります。
遠位指節間関節炎型
この型は、指先や爪の近くの小さな関節に影響を与えます。
特徴的な症状
- 指先の関節の痛みと腫れ
- 爪の変形や剥離
- 指先の「ソーセージ様」の腫れ(指炎)
関節炎性変形性関節症型
この型は、大きな関節に影響を及ぼし、変形性関節症に似た症状を示します。
| 症状 | 影響を受ける関節 |
| 痛みと腫れ | 膝、股関節、手首 |
| 関節の硬直 | 肘、足首 |
| 可動域の制限 | 肩 |
この型では、関節の破壊が進行する可能性があるため、早期発見と対応が不可欠です。
関節切断型
最も重度の型で、関節の著しい変形や破壊を引き起こす場合があります。
主な特徴
- 関節の重度の炎症
- 関節の変形
- 機能障害
- 極度の痛み
乾癬性関節炎の原因
乾癬性関節炎は、遺伝的要因と環境要因が複雑に絡み合って発症する自己免疫疾患です。単一の原因ではなく、複数の要素が組み合わさることで発症リスクが高まります。
遺伝的要因
乾癬性関節炎の発症には、遺伝子変異や多型が発症リスクを高めることが分かっています。
| 遺伝子 | 関連疾患 |
| HLA-B27 | 乾癬性関節炎、強直性脊椎炎 |
| IL-23R | 乾癬、炎症性腸疾患 |
| TNFAIP3 | 乾癬、関節リウマチ |
遺伝子は免疫系の調節に関与しており、変異があると過剰な免疫反応を引き起こします。
環境要因
発症に関する環境要因
- 感染症(特に上気道感染や皮膚感染)
- 外傷やケガ
- ストレス
- 喫煙
- 肥満
これらの要因は、体内の免疫系のバランスを崩し、自己免疫反応が起こります。
免疫系の異常
乾癬性関節炎の根本的な原因は、免疫系の機能異常です。
正常な免疫系は体を守る役割を果たしますが、乾癬性関節炎では免疫系が誤って自身の組織を攻撃します。
| 免疫細胞 | 役割 |
| T細胞 | 過剰活性化、炎症性サイトカイン産生 |
| 樹状細胞 | 異常な抗原提示 |
| マクロファージ | 炎症促進物質の分泌 |
炎症性サイトカイン
乾癬性関節炎の発症と進行は、TNF-α、IL-17、IL-23などの炎症性サイトカインが過剰に産生されることで起こります。
関節組織の破壊メカニズム
乾癬性関節炎では、持続的な炎症反応により関節組織が徐々に破壊されていきます。
過程に関与している要素
- 滑膜の肥厚と炎症
- 軟骨の分解
- 骨びらんの形成
- 新生骨の異常形成
乾癬性関節炎の検査・チェック方法
乾癬性関節炎の早期発見と正確な診断は、身体診察、画像診断、血液検査などを組み合わせて総合的に評価を行います。
身体診察
詳細な身体診察は、乾癬性関節炎の診断において基本となります。
| 診察項目 | 確認内容 |
| 皮膚の状態 | 乾癬の有無、程度、部位 |
| 関節の腫れ | 腫脹の有無、程度、対称性 |
| 関節の痛み | 圧痛の有無、部位 |
| 関節の可動域 | 制限の有無、程度 |
画像診断
画像診断は、関節の状態を詳細に評価するために用いられます。
- X線検査 骨びらんや関節の変形を確認
- MRI 初期の炎症や軟部組織の変化を検出
- 超音波検査 関節の滑膜肥厚や炎症の程度を評価
血液検査
血液検査は、炎症の程度や他の自己免疫疾患の可能性を評価するために行われます。
| 検査項目 | 評価内容 |
| CRP | 炎症の程度 |
| ESR | 炎症の程度 |
| RF | 関節リウマチとの鑑別 |
| 抗CCP抗体 | 関節リウマチとの鑑別 |
乾癬性関節炎の治療方法と治療薬について
乾癬性関節炎の治療は、、薬物療法を中心に、非薬物療法も組み合わせることで、患者さんの生活の質の向上を図ります。
非ステロイド性抗炎症薬(NSAIDs)
NSAIDsは、炎症を抑制し痛みをやわらげる効果があり、乾癬性関節炎の初期治療や軽度の症状管理に用いられます。
| 一般名 | 商品名の例 |
| イブプロフェン | ブルフェン |
| ナプロキセン | ナイキサン |
| セレコキシブ | セレコックス |
NSAIDsは即効性があるものの、長期使用には注意が必要です。
疾患修飾性抗リウマチ薬(DMARDs)
DMARDsは、乾癬性関節炎の進行を遅らせる効果が期待できる薬剤です。
従来型DMARDsと生物学的DMARDsに大別され、免疫系を調整することで炎症を抑制します。
生物学的製剤
生物学的製剤は、特定の炎症性サイトカインや免疫細胞を標的とし、乾癬性関節炎の治療において画期的な進歩をもたらしました。
| 薬剤タイプ | 標的 | 代表的な薬剤名 |
| 抗TNF-α薬 | TNF-α | アダリムマブ、エタネルセプト |
| 抗IL-17薬 | IL-17 | セクキヌマブ、イキセキズマブ |
| 抗IL-23薬 | IL-23 | グセルクマブ、リサンキズマブ |
生物学的製剤は、従来の治療に反応しない重症例や進行性の症例に効果を発揮します。
ヤヌスキナーゼ(JAK)阻害薬
JAK阻害薬は、最新の治療選択肢の一つです。
細胞内のシグナル伝達を阻害することで炎症を抑制し、生物学的製剤と同等の効果が期待できます。
局所療法
皮膚症状に対しては、局所療法も重要な役割を果たします。
主な局所治療薬
- ステロイド外用薬
- ビタミンD3誘導体外用薬
- タクロリムス軟膏
外用薬は、皮膚の炎症や鱗屑を軽減する効果があります。
乾癬性関節炎の治療期間と予後
乾癬性関節炎は慢性疾患であり、治療期間と予後は個人差が大きく、一概に定めることは困難でが、早期診断と対応により、多くの患者さんが症状をコントロールし、良好な生活の質を維持できます。
治療期間の個別性
乾癬性関節炎の治療期間は、患者さんごとに大きく異なります。
治療期間に影響を与える要因
| 要因 | 影響 |
| 発症時期 | 早期発見・早期治療開始で予後改善 |
| 症状の重症度 | 重症例ほど長期の治療が必要 |
| 治療への反応性 | 個人差が大きく、効果的な治療法の選択が重要 |
| 生活習慣 | 適切な生活管理で症状コントロールが容易に |
多くの場合、症状が安定するまでに数か月から1年程度かかり、その後も、再燃を予防し症状をコントロールするために、継続的な対応が必要です。
予後に影響を与える因子
乾癬性関節炎の予後は、さまざまな要因によって左右されます。
- 早期診断と治療開始
- 定期的な経過観察と治療調整
- 患者さん自身による症状管理
- 合併症の予防と対策
- 新しい治療法の利用
長期的な経過と生活の質
乾癬性関節炎は長期的な管理が必要な疾患ですが、多くの患者さんは、症状をコントロールしながら通常の生活を送れます。
| 期間 | 目標 |
| 短期(〜1年) | 症状の安定化、急性炎症の抑制 |
| 中期(1〜5年) | 症状のコントロール維持、機能障害の予防 |
| 長期(5年〜) | 生活の質の維持、合併症の予防 |
再燃と寛解
乾癬性関節炎は、症状の再燃と寛解を繰り返すことがあります。
再燃のリスクを抑えるための注意点
- 定期的な通院と経過観察
- 処方された薬の適切な服用
- ストレス管理と十分な休養
- バランスの取れた食事と適度な運動
- 感染症の予防
薬の副作用や治療のデメリットについて
乾癬性関節炎の治療薬は効果的である一方、さまざまな副作用やデメリットを伴います。
非ステロイド性抗炎症薬(NSAIDs)の副作用
NSAIDsは広く使用される薬剤ですが、長期使用には注意が必要です。
胃腸障害は最も一般的な副作用の一つで、胃潰瘍や消化管出血のリスクが高まり、腎機能や心血管のリスクも増加する傾向があります。
| 副作用 | 発生頻度 |
| 胃腸障害 | 高い |
| 腎機能障害 | 中程度 |
| 心血管障害 | 低い~中程度 |
疾患修飾性抗リウマチ薬(DMARDs)のデメリット
DMARDsは長期的な疾患コントロールに有効ですが、副作用が報告されています。
- メトトレキサート 肝毒性や骨髄抑制を引き起こす場合があり、定期的な血液検査が必要です。
- サラゾスルファピリジン 消化器症状や皮疹、まれに重篤な血液障害が生じることがあります。
これらの薬剤は妊娠中や授乳中の使用が制限されるため、妊娠を希望する患者さんは注意が必要です。
生物学的製剤の副作用とリスク
生物学的製剤は高い効果を示す一方で、免疫系を抑制するため感染症のリスクが増加します。
特に結核や肝炎の再活性化に注意が必要で、治療開始前のスクリーニングが不可欠です。
| 薬剤タイプ | 主な副作用 |
| 抗TNF-α薬 | 感染症、注射部位反応 |
| 抗IL-17薬 | カンジダ感染、炎症性腸疾患 |
| 抗IL-23薬 | 感染症、注射部位反応 |
また、まれではありますが、悪性腫瘍のリスク増加も懸念されています。
ヤヌスキナーゼ(JAK)阻害薬の懸念点
JAK阻害薬は比較的新しい薬剤であり、長期的な安全性データが限られています。
副作用や懸念点
- 感染症リスクの増加
- 血栓症のリスク上昇
- 脂質プロファイルの悪化
- 肝酵素上昇
高齢者や心血管リスクの高い患者さんでは、慎重に使用することが大切です。
局所療法の限界と副作用
ステロイド外用薬の長期使用は、皮膚萎縮や毛細血管拡張などの局所的副作用を引き起こす場合があり、ビタミンD3誘導体外用薬では、まれに高カルシウム血症が生じることがあります。
これらの局所療法は、広範囲の病変や関節症状には効果が限定的です。
保険適用と治療費
以下に記載している治療費(医療費)は目安であり、実際の費用は症状や治療内容、保険適用否により大幅に上回ることがございます。当院では料金に関する以下説明の不備や相違について、一切の責任を負いかねますので、予めご了承ください。
健康保険の適用範囲
乾癬性関節炎の治療は、通常の外来診療や入院治療、多くの薬剤治療が保険適用の対象となっていますが、一部の新しい治療法や特殊な検査には制限があります。
一般的な治療費の目安
治療費は、選択する治療法や通院頻度によって大きく変わります。
| 治療法 | 概算費用(3割負担の場合) |
| 外来診療(月1回) | 1,000〜3,000円 |
| 非ステロイド性抗炎症薬(1ヶ月分) | 2,000〜5,000円 |
| 生物学的製剤(1回投与) | 30,000〜100,000円 |
| リハビリテーション(1回) | 1,500〜3,000円 |
保険適用外の治療について
一部の最新治療法や代替療法は、保険適用外です。
| 治療法 | 概算費用(自己負担) |
| 特殊な光線療法 | 5,000〜15,000円/回 |
| 一部の漢方治療 | 10,000〜30,000円/月 |
| 最新の生物学的製剤(適応外使用) | 100,000〜300,000円/回 |
以上
参考文献
Moll JM, Wright V. Psoriatic arthritis. InSeminars in arthritis and rheumatism 1973 Jan 1 (Vol. 3, No. 1, pp. 55-78). WB Saunders.
Gladman DD. Psoriatic arthritis. Rheumatic Disease Clinics of North America. 1998 Nov 1;24(4):829-44.
Ritchlin CT, Colbert RA, Gladman DD. Psoriatic arthritis. New England Journal of Medicine. 2017 Mar 9;376(10):957-70.
Veale DJ, Fearon U. The pathogenesis of psoriatic arthritis. The Lancet. 2018 Jun 2;391(10136):2273-84.
FitzGerald O, Ogdie A, Chandran V, Coates LC, Kavanaugh A, Tillett W, Leung YY, deWit M, Scher JU, Mease PJ. Psoriatic arthritis. Nature reviews Disease primers. 2021 Aug 12;7(1):59.
Ogdie A, Weiss P. The epidemiology of psoriatic arthritis. Rheumatic Disease Clinics. 2015 Nov 1;41(4):545-68.
Scarpa R, ORIENTE P, PUCINO A, TORELLA M, VIGNONE L, RICCIO A, ORIENTE CB. Psoriatic arthritis in psoriatic patients. Rheumatology. 1984 Nov 1;23(4):246-50.
Mease P, Goffe BS. Diagnosis and treatment of psoriatic arthritis. Journal of the American Academy of Dermatology. 2005 Jan 1;52(1):1-9.
Duarte GV, Faillace C, De Carvalho JF. Psoriatic arthritis. Best Practice & Research Clinical Rheumatology. 2012 Feb 1;26(1):147-56.
Cantini F, Niccoli L, Nannini C, Kaloudi O, Bertoni M, Cassara E. Psoriatic arthritis: a systematic review. International journal of rheumatic diseases. 2010 Oct;13(4):300-17.
Van den Bosch F, Coates L. Clinical management of psoriatic arthritis. The Lancet. 2018 Jun 2;391(10136):2285-94.