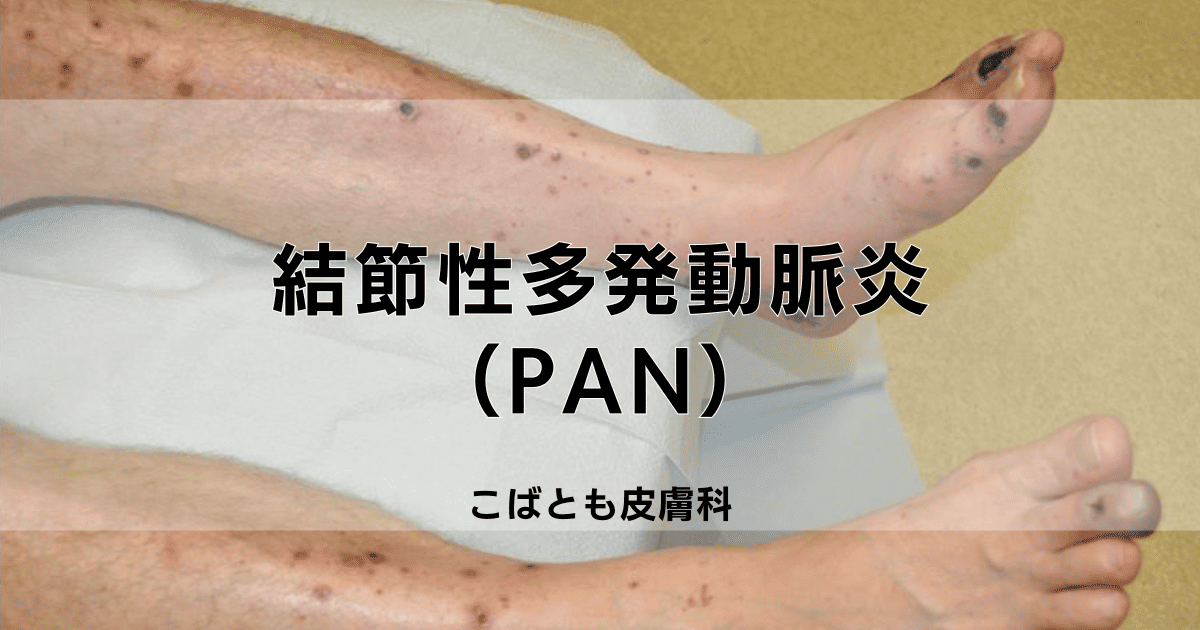
結節性多発動脈炎(PAN)(polyarteritis nodosa)とは、全身の中型・小型の動脈に炎症が生じる血管炎症候群の一つで、血管壁への炎症により血管の狭窄や閉塞が起こります。
この疾患は免疫システムが自己の血管組織を誤って攻撃する自己免疫疾患で、発症機序の詳細については現在も研究が進められています。
発熱や著明な体重減少、全身倦怠感などの全身症状に加え、皮膚、腎臓、末梢神経、消化器など複数の臓器に多彩な症状を引き起こすことが特徴的です。
この記事の執筆者

小林 智子(こばやし ともこ)
日本皮膚科学会認定皮膚科専門医・医学博士
こばとも皮膚科院長
2010年に日本医科大学卒業後、名古屋大学医学部皮膚科入局。同大学大学院博士課程修了後、アメリカノースウェスタン大学にて、ポストマスターフェローとして臨床研究に従事。帰国後、同志社大学生命医科学部アンチエイジングリサーチセンターにて、糖化と肌について研究を行う。専門は一般皮膚科、アレルギー、抗加齢、美容皮膚科。雑誌を中心にメディアにも多数出演。著書に『皮膚科医が実践している 極上肌のつくり方』(彩図社)など。
こばとも皮膚科関連医療機関
結節性多発動脈炎 (PAN)の症状
結節性多発動脈炎(PAN)は、中小型の動脈に炎症が生じ、全身のさまざまな臓器に多彩な症状をもたらします。
初期症状と全身症状
結節性多発動脈炎の初期段階では、発熱や全身倦怠感、体重減少といった非特異的な症状が現れることが多く、このような症状は他の膠原病や感染症でも見られるため、早期発見には詳しい問診と経過観察が重要です。
初期から中期にかけては、38度以上の発熱が数週間から数か月にわたって持続し、この間に筋肉痛や関節痛を伴うことで、日常生活に支障をきたす患者さんも少なくありません。
| 全身症状 | 頻度 | 特徴 |
|---|---|---|
| 発熱 | 高頻度 | 長期持続 |
| 体重減少 | 中頻度 | 食欲不振を伴う |
| 筋肉痛 | 高頻度 | 四肢に多い |
| 関節痛 | 中頻度 | 移動性 |
臓器別症状の特徴
結節性多発動脈炎では、血管炎により様々な臓器に血流障害が起こるため、それぞれの臓器特有の症状が出現します。
腎臓では、糸球体や細動脈に炎症が及ぶことで腎機能障害が生じ、高血圧や蛋白尿、血尿などの症状が見られることがあります。
消化器系では、腹痛や下痢、吐き気などの症状が現れ、食後の腹痛は腸管の血流障害によって起こる虚血性の痛みである可能性が高いです。
神経系の症状としては、末梢神経障害が特徴的で、手足のしびれや痛み、筋力低下などが左右非対称に現れます。
- 腎臓症状 高血圧、蛋白尿、血尿、浮腫
- 消化器症状 腹痛、下痢、吐き気、食欲不振
- 神経症状 末梢神経障害、しびれ、筋力低下
- 皮膚症状 皮下結節、紫斑、潰瘍、網状皮斑
皮膚症状と末梢循環障害
皮膚における結節性多発動脈炎の症状は、疾患の活動性を反映する重要な指標で、皮下結節は下肢に好発し、触診で硬い腫瘤として触れることができ、時に圧痛を伴います。
末梢循環障害による症状は、手足の冷感やしびれ、レイノー現象などが出現し、重症例では指趾に潰瘍が形成されることもあります。
| 皮膚症状 | 特徴 | 好発部位 |
|---|---|---|
| 皮下結節 | 圧痛性 | 下肢 |
| 紫斑 | 点状出血 | 四肢 |
| 潰瘍 | 難治性 | 指趾 |
| 網状皮斑 | 網目状 | 四肢 |
進行期の症状と合併症
結節性多発動脈炎が進行すると、複数の臓器症状が同時に生じることがあり、心臓、腎臓、神経系の症状が重なると予後に影響を及ぼします。
心臓では、冠動脈炎による狭心症様症状や不整脈が出現することがあり、胸痛や動悸、息切れなどの症状に注意が必要です。
眼症状としては、網膜動脈の血管炎による視力障害や視野欠損が起こり、急激な視力低下を訴える場合は速やかな対応が求められます。
肺症状はまれですが、間質性肺炎や胸水貯留などが見られることがあり、咳嗽や呼吸困難感などの症状が現れます。
- 心臓症状 胸痛、動悸、息切れ、不整脈
- 眼症状 視力低下、視野欠損、結膜充血
- 肺症状 咳嗽、呼吸困難、胸水
- 筋骨格症状 筋力低下、関節痛、筋肉痛
結節性多発動脈炎 (PAN)の原因
結節性多発動脈炎(PAN)は、免疫システムが自己の血管組織を誤って攻撃することで発症する自己免疫疾患であり、中型・小型の動脈に炎症が生じることが原因です。
免疫システムの異常と自己抗体
免疫システムの異常は、結節性多発動脈炎(PAN)の発症において最も重要な要因で、自己抗体の産生や免疫複合体の形成により血管壁への持続的な炎症反応を起こします。
免疫反応の異常により、血管内皮細胞が損傷を受け、血管壁の炎症や壊死が進行していくことで、様々な臓器に影響を及ぼすのです。
特に注目すべき点として、抗好中球細胞質抗体(ANCA)という自己抗体が一部の患者さんで検出されることがあり、これが血管炎の進行に関与している可能性が指摘されています。
| 自己抗体の種類 | 検出率 | 臨床的意義 |
|---|---|---|
| MPO-ANCA | 約10% | 腎臓病変との関連 |
| PR3-ANCA | 稀 | 血管炎の活動性 |
| その他の自己抗体 | 様々 | 病態の多様性 |
遺伝的要因と環境因子
遺伝的背景は結節性多発動脈炎の発症リスクを高める可能性があり、特定のHLA型との関連性が報告されて、環境因子との相互作用により、遺伝的素因を持つ人々がより発症しやすい傾向にあることが、明らかになってきました。
- HLA-DRB1*09
- HLA-DRB1*01
- IL-1β遺伝子多型
- TNF-α遺伝子多型
- IL-6遺伝子多型
感染症との関連性
B型肝炎ウイルス(HBV)感染は、結節性多発動脈炎の発症と強い関連性を持つことが知られており、特に発展途上国における発症要因です。
ウイルス感染に対する免疫応答の過程で免疫複合体が形成され血管壁に沈着することで、炎症反応が惹起されると考えられています。
| 関連する感染症 | 関連の強さ | 発症メカニズム |
|---|---|---|
| B型肝炎 | 強い | 免疫複合体形成 |
| パルボウイルスB19 | 中程度 | 血管内皮障害 |
| HIV | 弱い | 免疫異常惹起 |
環境要因と生活習慣
環境中の様々な因子が結節性多発動脈炎の発症や増悪に関与している可能性があり、特定の薬剤への曝露や職業性要因などが危険因子です。
また、喫煙や過度の飲酒、慢性的なストレスなどの生活習慣も、免疫システムに影響を与え、発症リスクを高めます。
- 特定の薬剤への曝露
- 職業性の化学物質
- 大気汚染物質
- 紫外線への過度の曝露
- 慢性的なストレス
環境要因は単独ではなく、遺伝的素因や他の危険因子と相互に作用することで、結節性多発動脈炎の発症リスクを増大させます。
結節性多発動脈炎 (PAN)の検査・チェック方法
結節性多発動脈炎(PAN)の診断には、問診や身体所見に加えて、血液・尿検査、画像検査、そして確定診断のための生検など、複数の検査を組み合わせた総合的な評価が重要です。
初診時の問診と身体診察
問診では、発熱や全身倦怠感などの全身症状の経過、筋肉痛や関節痛の有無、消化器症状や神経症状など、多岐にわたる症状について確認することが大切です。
身体診察では、皮下結節の触診、末梢神経障害の有無、筋力低下の程度、関節の腫脹や圧痛などを丁寧に確認していきます。
血圧測定は診察の基本となり、結節性多発動脈炎では高血圧を伴うことが多いため、両腕での測定値の違いにも注意を払います。
| 問診項目 | 確認内容 | 評価のポイント |
|---|---|---|
| 全身症状 | 発熱・倦怠感 | 持続期間・程度 |
| 筋骨格症状 | 筋肉痛・関節痛 | 部位・性質 |
| 消化器症状 | 腹痛・食欲不振 | 発現時期・頻度 |
| 神経症状 | しびれ・脱力 | 左右差・進行性 |
血液検査と尿検査による評価
血液検査では、炎症マーカーであるCRPや赤沈値の上昇、貧血の有無、肝機能や腎機能の評価を行い、結節性多発動脈炎(PAN)の活動性や臓器障害の程度を判断します。
免疫学的検査として、抗好中球細胞質抗体(ANCA)の測定を行いますが、結節性多発動脈炎ではANCAが陰性となることが多く、他の血管炎症候群との鑑別に有用です。
補体価の測定も実施し、C3やC4の低下が見られる際には、免疫複合体による血管炎の可能性を考慮します。
- 一般血液検査 白血球数、赤血球数、血小板数、CRP、赤沈値
- 生化学検査 肝機能、腎機能、電解質、CK
- 免疫学的検査 ANCA、抗核抗体、補体価、免疫複合体
- 感染症検査 B型肝炎ウイルス、C型肝炎ウイルス
画像検査による血管病変の評価
血管造影検査は結節性多発動脈炎の診断において非常に大切で、特徴的な動脈瘤や狭窄性病変の有無を確認することが可能です。
CT検査やMRI検査では、臓器の血流障害や梗塞巣の有無、動脈瘤の存在などを詳細に観察することが可能で、超音波検査は末梢血管の評価に優れており、血管壁の肥厚や血流障害の程度を調べられます。
| 画像検査 | 主な評価項目 | 特徴 |
|---|---|---|
| 血管造影 | 動脈瘤・狭窄 | 確定診断に有用 |
| CT/MRI | 臓器障害・血流評価 | 全身評価可能 |
| 超音波 | 血管壁肥厚・血流障害 | 非侵襲的 |
生検による確定診断
確定診断のためには、可能な限り罹患血管の生検を行い、病理組織学的検査によって血管炎の存在を証明することが不可欠です。
皮膚生検は比較的安全に実施できる検査法で、皮下結節や紫斑が出現している部位から組織を採取し、中小型動脈の血管炎の有無を確認します。
筋生検も診断に役立ち、筋症状が強い部位や、筋電図で異常が認められた部位からの組織採取を行います。
- 皮膚生検 皮下結節、紫斑部位からの採取
- 筋生検 症状のある筋肉からの採取
- 神経生検 末梢神経障害部位からの採取
- 腎生検 腎機能障害時の評価
結節性多発動脈炎 (PAN)の治療法と治療薬について
結節性多発動脈炎(PAN)の治療では、ステロイド薬による寛解導入療法を基本とし、重症例では免疫抑制薬を併用しながら、通常6ヶ月から2年程度の治療期間を要します。
初期治療(寛解導入療法)
副腎皮質ステロイド薬による治療は結節性多発動脈炎の治療において最も重要で、多くの場合、プレドニゾロンを1日0.5-1mg/kgの高用量から開始します。
初期治療では、炎症を抑制し急性期の症状を改善させることを目的として、十分な量のステロイド薬を使用することが必要です。
重症例や予後不良因子を有する患者さんでは、シクロホスファミドなどの免疫抑制薬を併用することで、より確実な効果を得られます。
| 治療薬 | 投与量 | 投与期間 |
|---|---|---|
| プレドニゾロン | 0.5-1mg/kg/日 | 4-8週間 |
| シクロホスファミド | 2mg/kg/日 | 3-6ヶ月 |
| アザチオプリン | 1-2mg/kg/日 | 維持期に使用 |
維持療法
初期治療で症状が改善した後は、ステロイド薬を徐々に減量しながら、再燃予防のための維持療法へと移行します。
維持療法期間中は、症状の再燃や副作用の出現に注意を払いながら、慎重に投薬量を調整していくことが大切です。
- メトトレキサート(週1回投与)
- ミゾリビン(1日2-3回分割投与)
- タクロリムス(1日2回分割投与)
重症例への対応
臓器障害が進行している重症例では、ステロイドパルス療法やシクロホスファミドの静脈内投与など、より強力な免疫抑制療法を選択することがあります。
血漿交換療法は、重症例や従来の治療に反応が乏しい場合の治療選択肢として考慮され、免疫複合体の除去による症状改善を期待できます。
| 治療法 | 適応 | 期待される効果 |
|---|---|---|
| ステロイドパルス | 重症例 | 急速な炎症抑制 |
| 血漿交換 | 難治例 | 免疫複合体除去 |
| 大量免疫グロブリン | 重症例 | 免疫調節作用 |
治療経過のモニタリング
定期的な血液検査や尿検査を通じて、炎症マーカーの推移や臓器機能の変化を詳細に評価していくことが大切です。
治療効果の判定には、CRPや赤沈などの炎症マーカーの変動、臨床症状の推移、画像検査による血管病変の評価など、複数の指標を総合的に用います。
- 血液検査(CRP、赤沈、血算、腎機能など)
- 尿検査(蛋白尿、潜血など)
- 画像検査(血管造影、CT、MRIなど)
副腎皮質ステロイド薬の長期使用に伴う副作用の出現にも十分な注意が必要で、骨粗鬆症予防薬の併用や感染症予防などの対策を講じます。
薬の副作用や治療のデメリットについて
結節性多発動脈炎(PAN)の治療では、主にステロイド薬や免疫抑制薬を使用しますが、薬剤には感染症のリスク増加や骨粗鬆症などの様々な副作用が伴います。
ステロイド薬による副作用
ステロイド薬の長期使用では、免疫機能の低下により日和見感染症にかかりやすくなるため、肺炎球菌やニューモシスチス肺炎などの呼吸器感染症に注意が必要です。
骨代謝への影響も顕著で、閉経後の女性や高齢者では骨粗鬆症の発症や進行が加速することがあり、骨折のリスクも上昇します。
消化器系への影響として、胃潰瘍や十二指腸潰瘍などの消化性潰瘍が発生することがあり、非ステロイド性抗炎症薬(NSAIDs)と併用する際には出血のリスクが高まります。
| 副作用 | 症状・所見 | 好発時期 |
|---|---|---|
| 骨粗鬆症 | 骨密度低下 | 3ヶ月以降 |
| 消化性潰瘍 | 腹痛・出血 | 使用初期 |
| 糖尿病 | 血糖上昇 | 1ヶ月以降 |
| 高血圧 | 血圧上昇 | 使用初期 |
免疫抑制薬による副作用
シクロホスファミドなどの免疫抑制薬では、骨髄抑制による白血球減少や血小板減少が起こりやすく、重症感染症や出血のリスクが増加します。
長期使用による発がんリスクの上昇も指摘されており、膀胱がんや血液系悪性腫瘍の発生には注意深い経過観察が欠かせません。
不妊や生殖機能への影響も報告されており、若年患者さんへの使用に際しては、将来の妊孕性への影響について十分な説明と対策を講じる必要があります。
- 血液毒性 白血球減少、血小板減少、貧血
- 生殖毒性 不妊、月経異常、精子形成障害
- 発がんリスク 膀胱がん、血液がん、二次性悪性腫瘍
- 肝毒性 肝機能障害、黄疸、肝炎
生物学的製剤による副作用
生物学的製剤の使用では、従来の免疫抑制薬とは異なる特有の副作用が出現する可能性があり、結核などの日和見感染症の発症リスクがあります。
投与部位反応として、注射部位の発赤や腫脹、かゆみなどが生じることがありますが、症状は一般的に一過性であり、経過とともに改善することが多いです。
アレルギー反応や過敏症状として、投与中や投与直後に発熱、発疹、呼吸困難などが現れることがあります。
| 副作用 | 初期症状 | 対処方法 |
|---|---|---|
| 感染症 | 発熱・咳 | 投与中止 |
| アレルギー | 発疹・掻痒 | 減速・中止 |
| 注射部位反応 | 発赤・腫脹 | 経過観察 |
| 自己抗体産生 | 関節痛・発熱 | 用量調整 |
併用薬による相互作用と副作用
複数の薬剤を併用することで、それぞれの副作用が増強されたり、新たな副作用が現れたりする場合があります。
非ステロイド性抗炎症薬(NSAIDs)とステロイド薬の併用では、消化管出血のリスクが著しく上昇することがあり、また、感染症予防のための抗生物質の長期使用は、耐性菌の出現や腸内細菌叢の乱れを引き起こします。
- 消化管への影響 出血、潰瘍、穿孔
- 腎機能への影響 急性腎障害、電解質異常
- 肝機能への影響 薬物性肝障害、胆汁うっ滞
- 血液凝固系への影響 出血傾向、血栓形成
保険適用と治療費
以下に記載している治療費(医療費)は目安であり、実際の費用は症状や治療内容、保険適用否により大幅に上回ることがございます。当院では料金に関する以下説明の不備や相違について、一切の責任を負いかねますので、予めご了承ください。
外来診療における治療費
定期的な外来診療では、血液検査や尿検査などの臨床検査に加え、画像診断や投薬が必要です。
| 診療項目 | 自己負担額(3割負担の場合) |
|---|---|
| 血液検査 | 3,000円~5,000円 |
| 尿検査 | 1,000円~2,000円 |
| CT検査 | 9,000円~15,000円 |
| MRI検査 | 15,000円~25,000円 |
投薬治療にかかる費用
- ステロイド薬(プレドニゾロン) 月額 2,000円~4,000円
- 免疫抑制薬(シクロホスファミド) 月額 5,000円~10,000円
- 生物学的製剤 月額 30,000円~50,000円
検査・モニタリングの費用
定期的なモニタリング検査は結節性多発動脈炎(PAN)の活動性評価や治療効果の判定に不可欠です。
| 検査種類 | 検査間隔 | 自己負担額(3割負担) |
|---|---|---|
| 定期血液検査 | 1-3ヶ月毎 | 3,000円~5,000円 |
| 血管造影検査 | 必要時 | 20,000円~30,000円 |
| 超音波検査 | 3-6ヶ月毎 | 3,000円~6,000円 |
以上
参考文献
De Virgilio A, Greco A, Magliulo G, Gallo A, Ruoppolo G, Conte M, Martellucci S, de Vincentiis M. Polyarteritis nodosa: a contemporary overview. Autoimmunity reviews. 2016 Jun 1;15(6):564-70.
Forbess L, Bannykh S. Polyarteritis nodosa. Rheumatic Disease Clinics. 2015 Feb 1;41(1):33-46.
Morgan AJ, Schwartz RA. Cutaneous polyarteritis nodosa: a comprehensive review. International journal of dermatology. 2010 Jul;49(7):750-6.
Stone JH. Polyarteritis nodosa. Jama. 2002 Oct 2;288(13):1632-9.
Hernández-Rodríguez J, Alba MA, Prieto-González S, Cid MC. Diagnosis and classification of polyarteritis nodosa. Journal of autoimmunity. 2014 Feb 1;48:84-9.
Bauza A, España A, Idoate M. Cutaneous polyarteritis nodosa. British Journal of Dermatology. 2002 Apr 1;146(4):694-9.
BORRIE P. Cutaneous polyarteritis nodosa. British Journal of Dermatology. 1972 Aug;87(2):87-95.
Howard T, Ahmad K, Swanson JA, Misra S. Polyarteritis nodosa. Techniques in vascular and interventional radiology. 2014 Dec 1;17(4):247-51.
Chen KR. Cutaneous polyarteritis nodosa: a clinical and histopathological study of 20 cases. The Journal of dermatology. 1989 Dec;16(6):429-42.
Nakamura T, Kanazawa N, Ikeda T, Yamamoto Y, Nakabayashi K, Ozaki S, Furukawa F. Cutaneous polyarteritis nodosa: revisiting its definition and diagnostic criteria. Archives of Dermatological Research. 2009 Jan;301:117-21.